Bo có 2 đồng vị là 10B và 11B với nguyên tử khối trung bình là 10,81. Thành phần % về khối lượng của đồng vị 11B chứa trong H3BO3 là (Cho: H = 1, O = 16)
A. 14,00%.
B. 14,16%.
C. 14,42%.
D. 15,00%.
Trong tự nhiên nguyên tố Bo có hai đồng vị bền là 11B và 10B. Biết nguyên tử khối trung bình của Bo là 10,81. Trung bình cứ có 1539 nguyên tử 10B thì sẽ có tương ứng bao nhiêu nguyên tử 11B ?
A. 292
B. 361
C. 1247
D. 6561
Đáp án D
• Giả sử % nguyên tử 11B và 10B trong tự nhiên lần lượt là x, y.
Ta có hpt:
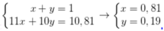
Nếu có 1539 nguyên tử 10B thì có
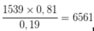 nguyên tử 11B.
nguyên tử 11B.
trong tự nhiên Bo có 2 đồng vị là 10B và 11B. Khối lượng nguyên tử trung bình của Bo là 110,82u. Mỗi khi có 73 nguyên tử 10B thì có bao nhiêu nguyên tử 11B ???
rong tự nhiên Bo có 2 đồng vị là 10B và 11B. Khối lượng nguyên tử trung bình của Bo là 10,82u. Mỗi khi có 73 nguyên tử 10B thì có bao nhiêu nguyên tử 11B ???
x là phần trăm của 10B.
Khối lượng trung bình 10,82= \(\frac{10x+11\left(100-x\right)}{100}\)
Tính ra %10B = 18%. %11B= 82%.
Tỉ lệ \(\frac{\%10B}{\%11B}=\frac{9}{41}\)
Từ tỉ lệ này tính thì 73 nguyên tử 10B có \(\frac{73\cdot41}{9}\simeq332.5\) nguyên tử 11B.
Thế kết quả vào kiểm tra lại Khối lượng trung bình của B là 10,8199 .
Chúc bạn học học tốt![]()
khối lượng nguyên tử của b bằng 10.81. b trong tự nhiên gồm hai đồng vị 10b và 11b. hỏi có bao nhiêu phần trăm 11b trong axit boric H3BO. Cho H3BO3 = 61,81
Bo có 2 đồng vị là 10B và 11B với nguyên tử khối trung bình là 10,81. Một hợp chất có công thức BX3 (X là nguyên tố chưa biết, trong đó đồng vị 11B chiếm 13,14% khối lượng. Nguyên tố X là
A. H (1)
B. F (19)
C. Br (80)
D. Cl (35,5)
Bo có 2 đồng vị là 10B và 11B với nguyên tử khối trung bình là 10,81. Một hợp chất có công thức BX3 (X là nguyên tố chưa biết, trong đó đồng vị 11B chiếm 13,14% khối lượng. Nguyên tố X là
A. H (1)
B. F (19)
C. Br (80)
D. Cl (35,5)
Nguyên tố Bo có 2 đồng vị 11B (x1%) và 10B (x2%), ngtử khối trung bình của Bo là 10,8. Giá trị của x1% là:
A. 80%.
B. 20%.
C. 10,8%.
D. 89,2%.
Đáp án A
Gọi thành phần phần trăm của 11B và 10B lần lượt x, y
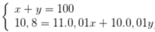
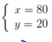
Phần trăm số nguyên tử của 11B là 80%
Nguyên tử khối trung bình của Clo là 35,5. Clo trong tự nhiên có hai đồng vị là 35 Cl và 37 Cl. Tính phần trăm về khối lượng của 37 Cl chứa trong HClO4 (với Hidro đồng vị là 1 H, oxi đồng vị là 16 O)
\(\%^{35}Cl=x\%\Rightarrow\%^{37}Cl=\left(100-x\right)\%\)
\(\overline{M}=\dfrac{35x+37\cdot\left(100\%-x\right)}{100\%}=35.5\left(g\text{/}mol\right)\)
\(\Rightarrow x=75\%\)
\(\%^{37}Cl_{\left(HClO_4\right)}=\dfrac{25\%\cdot37}{1+35.5+16\cdot4}\cdot100\%=9.2\%\)
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=
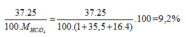
Bo có 2 đồng vị: 10B và 11B. Biết AB = 10,828 a. Tính % các đồng vị. b. Nếu có 50 nguyên tử 10B thì hỏi có bao nhiêu nguyên tử 11B, B?
trong từ nhiên B có 2 đồng vị10B và11B . n tử khối tb của bo là 10,81
a, tính phần trăm của mỗi đồng vị
b, tính phần trăm khối lượng11B trong H3BO3 (bt H là đv1H , O là đv16O )
a, Gọi x(%) là tỉ lệ số nguyên tử của 10B. ĐK: x>0.
Ta có: \(10.x\%+11\left(100-x\right)\%=10,81\)
\(\Leftrightarrow x=19\left(TM\right)\)(%)
\(\Rightarrow100-x=81\left(\%\right)\)
b, \(\%_{^{11}B}=\frac{11.81\%}{3+10,81+16.3}.100\)\(\approx14,42\left(\%\right)\)
#Walker